Ալցհայմերի հիվանդությունը, որը տարեցների շրջանում ամենատարածված դեպքն է, տանջում է մարդկանց մեծ մասին։
Ալցհայմերի հիվանդության բուժման մարտահրավերներից մեկն այն է, որ թերապևտիկ դեղամիջոցների ուղեղի հյուսվածքին մատակարարումը սահմանափակվում է արյունաուղեղային պատնեշով: Ուսումնասիրությունը պարզել է, որ ՄՌՏ-ուղեցույցով ցածր ինտենսիվությամբ ֆոկուսային ուլտրաձայնը կարող է շրջելիորեն բացել արյունաուղեղային պատնեշը Ալցհայմերի հիվանդությամբ կամ այլ նյարդաբանական խանգարումներով, այդ թվում՝ Պարկինսոնի հիվանդությամբ, ուղեղի ուռուցքներով և ամիոտրոֆիկ կողմնային սկլերոզով հիվանդների մոտ:
Արևմտյան Վիրջինիայի համալսարանի Ռոքֆելլերի նյարդաբանության ինստիտուտում վերջերս անցկացված փոքրածավալ փորձարկումը ցույց տվեց, որ Ալցհայմերի հիվանդությամբ հիվանդները, որոնք ստացել են ադուկանումաբի ներարկում կենտրոնացված ուլտրաձայնի հետ համատեղ, ժամանակավորապես բացել են արյուն-ուղեղային պատնեշը, ինչը զգալիորեն նվազեցրել է ուղեղի ամիլոիդ բետա (Aβ) բեռը փորձարկման փուլում: Հետազոտությունը կարող է նոր դռներ բացել ուղեղի խանգարումների բուժման համար:
Արյունաուղեղային պատնեշը պաշտպանում է ուղեղը վնասակար նյութերից՝ միաժամանակ թույլ տալով անհրաժեշտ սննդանյութերի անցումը: Սակայն արյունաուղեղային պատնեշը նաև կանխում է թերապևտիկ դեղամիջոցների ուղեղ մատակարարումը, ինչը հատկապես սուր մարտահրավեր է Ալցհայմերի հիվանդության բուժման ժամանակ: Աշխարհը ծերանալուն զուգընթաց, Ալցհայմերի հիվանդությամբ տառապող մարդկանց թիվը տարեցտարի ավելանում է, և դրա բուժման տարբերակները սահմանափակ են, ինչը ծանր բեռ է դնում առողջապահության վրա: Ադուկանումաբը ամիլոիդ բետա (Aβ) կապող մոնոկլոնալ հակամարմին է, որը հաստատվել է ԱՄՆ Սննդի և դեղերի վարչության (FDA) կողմից Ալցհայմերի հիվանդության բուժման համար, սակայն դրա ներթափանցումը արյունաուղեղային պատնեշով սահմանափակ է:
Կենտրոնացված ուլտրաձայնը առաջացնում է մեխանիկական ալիքներ, որոնք առաջացնում են սեղմման և նոսրացման միջև տատանումներ: Արյան մեջ ներարկվելիս և ուլտրաձայնային դաշտի ազդեցության տակ ընկնելիս փուչիկները սեղմվում և ընդարձակվում են ավելի շատ, քան շրջակա հյուսվածքն ու արյունը: Այս տատանումները մեխանիկական լարվածություն են ստեղծում արյան անոթի պատի վրա, ինչի հետևանքով էնդոթելային բջիջների միջև ամուր կապերը ձգվում և բացվում են (նկարը ստորև): Արդյունքում, արյուն-ուղեղային պատնեշի ամբողջականությունը խաթարվում է, ինչը թույլ է տալիս մոլեկուլներին դիֆուզիոն մտնել ուղեղ: Արյան-ուղեղային պատնեշը ինքնուրույն վերականգնվում է մոտ վեց ժամվա ընթացքում:
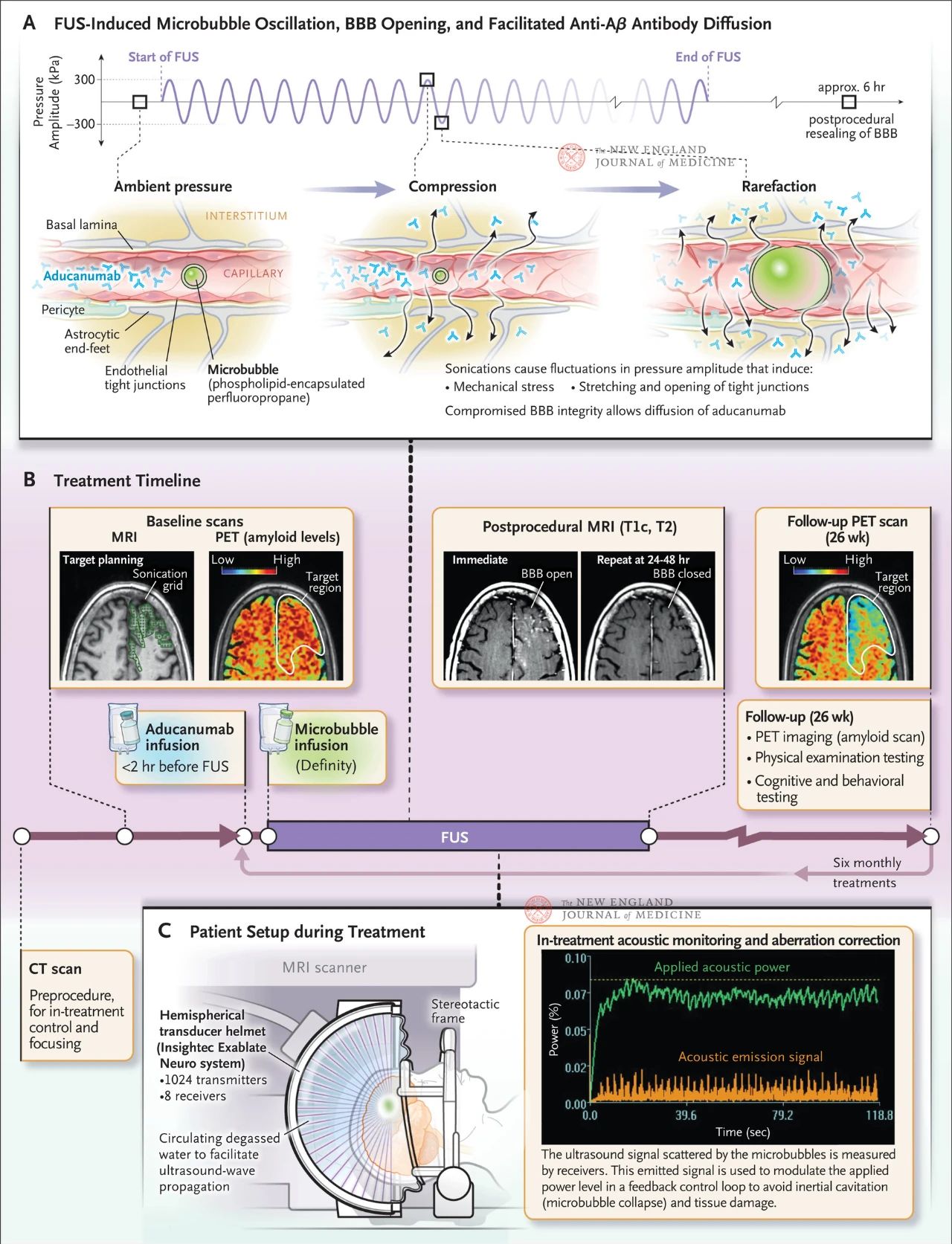
Նկարը ցույց է տալիս ուղղորդված ուլտրաձայնի ազդեցությունը մազանոթների պատերի վրա, երբ արյան անոթներում առկա են միկրոմետր չափի փուչիկներ: Գազի բարձր սեղմելիության պատճառով փուչիկները կծկվում և լայնանում են ավելի շատ, քան շրջակա հյուսվածքը, առաջացնելով մեխանիկական լարվածություն էնդոթելային բջիջների վրա: Այս գործընթացը առաջացնում է ամուր կապերի բացում և կարող է նաև հանգեցնել աստրոցիտների ծայրերի անկմանը արյան անոթի պատից, ինչը խաթարում է արյուն-ուղեղային պատնեշի ամբողջականությունը և նպաստում հակամարմինների դիֆուզիային: Բացի այդ, ֆոկուսացված ուլտրաձայնի ազդեցությանը ենթարկված էնդոթելային բջիջները ուժեղացրել են իրենց ակտիվ վակուոլային փոխադրման ակտիվությունը և ճնշել արտահոսքի պոմպի գործառույթը, դրանով իսկ նվազեցնելով ուղեղի հակամարմինների մաքրումը: Նկար B-ն ցույց է տալիս բուժման ժամանակացույցը, որը ներառում է համակարգչային տոմոգրաֆիա (CT) և մագնիսական ռեզոնանսային պատկերացում (MRI)՝ ուլտրաձայնային բուժման պլանը մշակելու համար, 18F-ֆլուբիտաբան պոզիտրոնային էմիսիոն տոմոգրաֆիա (PET)՝ սկզբնական փուլում, հակամարմինների ներարկում ֆոկուսացված ուլտրաձայնային բուժումից առաջ և միկրովեզիկուլյար ներարկում բուժման ընթացքում, ինչպես նաև բուժումը վերահսկելու համար օգտագործվող միկրովեզիկուլյար ցրող ուլտրաձայնային ազդանշանների ակուստիկ մոնիթորինգ: Ֆոկուսացված ուլտրաձայնային բուժումից հետո ստացված պատկերները ներառում էին T1-կշռված կոնտրաստային ուժեղացված ՄՌՏ, որը ցույց տվեց, որ արյուն-ուղեղային պատնեշը բաց էր ուլտրաձայնային մշակված տարածքում: Նույն տարածքի պատկերները 24-48 ժամ ֆոկուսացված ուլտրաձայնային բուժումից հետո ցույց տվեցին արյուն-ուղեղային պատնեշի լիակատար ապաքինում: 26 շաբաթ անց հիվանդներից մեկի հետազոտության ընթացքում կատարված 18F-ֆլուբիտաբան ՊԷՏ սկանավորումը ցույց տվեց ուղեղում Aβ մակարդակի նվազում բուժումից հետո: Նկար C-ն ցույց է տալիս ՄՌՏ ուղղորդմամբ ֆոկուսացված ուլտրաձայնային կառուցվածքը բուժման ընթացքում: Կիսագնդաձև փոխակերպիչի սաղավարտը պարունակում է ավելի քան 1000 ուլտրաձայնային աղբյուրներ, որոնք միավորվում են ուղեղի մեկ կիզակետում՝ օգտագործելով ՄՌՏ-ից իրական ժամանակի ուղղորդումը:
2001 թվականին կենդանիների վրա կատարված ուսումնասիրություններում առաջին անգամ ցույց տրվեց, որ կենտրոնացված ուլտրաձայնը բացում է արյուն-ուղեղային պատնեշը, և հետագա նախակլինիկական ուսումնասիրությունները ցույց են տվել, որ կենտրոնացված ուլտրաձայնը կարող է բարելավել դեղերի մատակարարումը և արդյունավետությունը: Այդ ժամանակվանից ի վեր պարզվել է, որ կենտրոնացված ուլտրաձայնը կարող է անվտանգ կերպով բացել արյուն-ուղեղային պատնեշը Ալցհայմերի հիվանդությամբ հիվանդների մոտ, ովքեր դեղորայք չեն ստանում, ինչպես նաև կարող է հակամարմիններ մատակարարել կրծքագեղձի քաղցկեղի ուղեղի մետաստազների դեմ:
Միկրոփուչիկների մատակարարման գործընթացը
Միկրոփուչիկները ուլտրաձայնային կոնտրաստային նյութ են, որը սովորաբար օգտագործվում է արյան հոսքը և արյան անոթները ուլտրաձայնային ախտորոշման ժամանակ դիտարկելու համար: Ուլտրաձայնային թերապիայի ընթացքում ներերակային ներարկվել է օկտաֆտորպրոպանի ֆոսֆոլիպիդով պատված ոչ պիրոգեն պղպջակների սուսպենզիա (Նկար 1Բ): Միկրոփուչիկները խիստ պոլիդիսպերսացված են, որոնց տրամագիծը տատանվում է 1 մկմ-ից պակասից մինչև 10 մկմ-ից ավելի: Օկտաֆտորպրոպանը կայուն գազ է, որը չի մետաբոլիզացվում և կարող է արտազատվել թոքերի միջոցով: Պղպջակները փաթաթող և կայունացնող լիպիդային թաղանթը կազմված է երեք բնական մարդկային լիպիդներից, որոնք մետաբոլիզացվում են էնդոգեն ֆոսֆոլիպիդների նման ձևով:
Կենտրոնացված ուլտրաձայնի ստեղծում
Ֆոկուսացված ուլտրաձայնը ստեղծվում է կիսագնդաձև փոխակերպիչ սաղավարտի միջոցով, որը շրջապատում է հիվանդի գլուխը (Նկար 1C): Սաղավարտը հագեցած է 1024 անկախ կառավարվող ուլտրաձայնային աղբյուրներով, որոնք բնականաբար ֆոկուսավորված են կիսագնդի կենտրոնում: Այս ուլտրաձայնային աղբյուրները սնուցվում են սինուսոիդալ ռադիոհաճախականության լարումներով և արձակում են մագնիսական ռեզոնանսային պատկերմամբ ուղղորդվող ուլտրաձայնային ալիքներ: Հիվանդը կրում է սաղավարտ, և գազազերծված ջուրը շրջանառվում է գլխի շուրջ՝ ուլտրաձայնի փոխանցումը հեշտացնելու համար: Ուլտրաձայնը մաշկի և գանգի միջով անցնում է ուղեղի թիրախին:
Գանգի հաստության և խտության փոփոխությունները կազդեն ուլտրաձայնի տարածման վրա, ինչը կհանգեցնի ուլտրաձայնի վնասվածքին հասնելու մի փոքր տարբեր ժամանակի: Այս աղավաղումը կարելի է շտկել՝ ձեռք բերելով բարձր թույլտվությամբ համակարգչային տոմոգրաֆիայի տվյալներ՝ գանգի ձևի, հաստության և խտության մասին տեղեկատվություն ստանալու համար: Համակարգչային սիմուլյացիայի մոդելը կարող է հաշվարկել յուրաքանչյուր շարժիչ ազդանշանի փոխհատուցված փուլային տեղաշարժը՝ սուր ֆոկուսը վերականգնելու համար: Ռադիոհաճախականության ազդանշանի փուլը կառավարելով՝ ուլտրաձայնը կարող է էլեկտրոնային եղանակով ֆոկուսավորվել և տեղադրվել՝ հյուսվածքի մեծ քանակություն ծածկելու համար՝ առանց ուլտրաձայնային աղբյուրի զանգվածը տեղաշարժելու: Նպատակային հյուսվածքի գտնվելու վայրը որոշվում է գլխի մագնիսական ռեզոնանսային պատկերմամբ՝ սաղավարտ կրելիս: Նպատակային ծավալը լցված է ուլտրաձայնային խարիսխային կետերի եռաչափ ցանցով, որոնք 5-10 մվրկ-ով արձակում են ուլտրաձայնային ալիքներ յուրաքանչյուր խարիսխային կետում, կրկնվելով յուրաքանչյուր 3 վայրկյանը մեկ: Ուլտրաձայնային հզորությունը աստիճանաբար մեծանում է մինչև ցանկալի պղպջակների ցրման ազդանշանի հայտնաբերումը, ապա պահվում է 120 վայրկյան: Այս գործընթացը կրկնվում է այլ ցանցերի վրա, մինչև թիրախային ծավալը լիովին ծածկվի:
Արյունաուղեղային պատնեշի բացումը պահանջում է, որ ձայնային ալիքների ամպլիտուդը գերազանցի որոշակի շեմ, որից այն կողմ պատնեշի թափանցելիությունը մեծանում է ճնշման ամպլիտուդի աճին զուգընթաց, մինչև հյուսվածքների վնասումը տեղի ունենա, որը դրսևորվում է որպես էրիթրոցիտների էկզոսմոզ, արյունահոսություն, ապոպտոզ և նեկրոզ, որոնք բոլորը հաճախ կապված են պղպջակների փլուզման հետ (կոչվում է իներցիոն կավիտացիա): Շեմը կախված է միկրոպղպջակների չափից և թաղանթի նյութից: Միկրոպղպջակների կողմից ցրված ուլտրաձայնային ազդանշանները հայտնաբերելով և մեկնաբանելով՝ ազդեցությունը կարող է պահվել անվտանգ միջակայքում:
Ուլտրաձայնային բուժումից հետո, T1-կշռված ՄՌՏ հետազոտությունը կոնտրաստային նյութով կիրառվել է որոշելու համար, թե արդյոք արյուն-ուղեղային պատնեշը բաց է թիրախային հատվածում, իսկ T2-կշռված պատկերները օգտագործվել են հաստատելու համար, թե արդյոք տեղի է ունեցել էքստրավազացիա կամ արյունահոսություն: Այս դիտարկումները ուղեցույց են հանդիսանում անհրաժեշտության դեպքում այլ բուժումները ճշգրտելու համար:
Թերապևտիկ ազդեցության գնահատումը և հեռանկարը
Հետազոտողները քանակականացրել են բուժման ազդեցությունը ուղեղի Aβ բեռի վրա՝ համեմատելով 18F-ֆլուբիտաբան պոզիտրոնային էմիսիոն տոմոգրաֆիան բուժումից առաջ և հետո՝ գնահատելու համար Aβ ծավալի տարբերությունը բուժված հատվածի և հակառակ կողմում գտնվող նմանատիպ A հատվածի միջև: Նույն թիմի կողմից նախորդ հետազոտությունները ցույց են տվել, որ պարզապես ուլտրաձայնի կենտրոնացումը կարող է փոքր-ինչ նվազեցնել Aβ մակարդակը: Այս փորձարկման ընթացքում դիտարկված նվազումն ավելի մեծ էր, քան նախորդ ուսումնասիրություններում:
Ապագայում ուղեղի երկու կողմերում բուժման ընդլայնումը կարևոր կլինի հիվանդության զարգացումը հետաձգելու արդյունավետությունը գնահատելու համար: Բացի այդ, անհրաժեշտ են ավելի շատ հետազոտություններ՝ երկարաժամկետ անվտանգությունն ու արդյունավետությունը որոշելու համար, և ավելի լայն հասանելիության համար պետք է մշակվեն ծախսարդյունավետ թերապևտիկ սարքեր, որոնք չեն հիմնվում առցանց ՄՌՏ ուղեցույցի վրա: Այնուամենայնիվ, արդյունքները լավատեսություն են ներշնչել, որ Aβ-ն վերացնող բուժումը և դեղամիջոցները կարող են ի վերջո դանդաղեցնել Ալցհայմերի զարգացումը:
Հրապարակման ժամանակը. Հունվար-06-2024