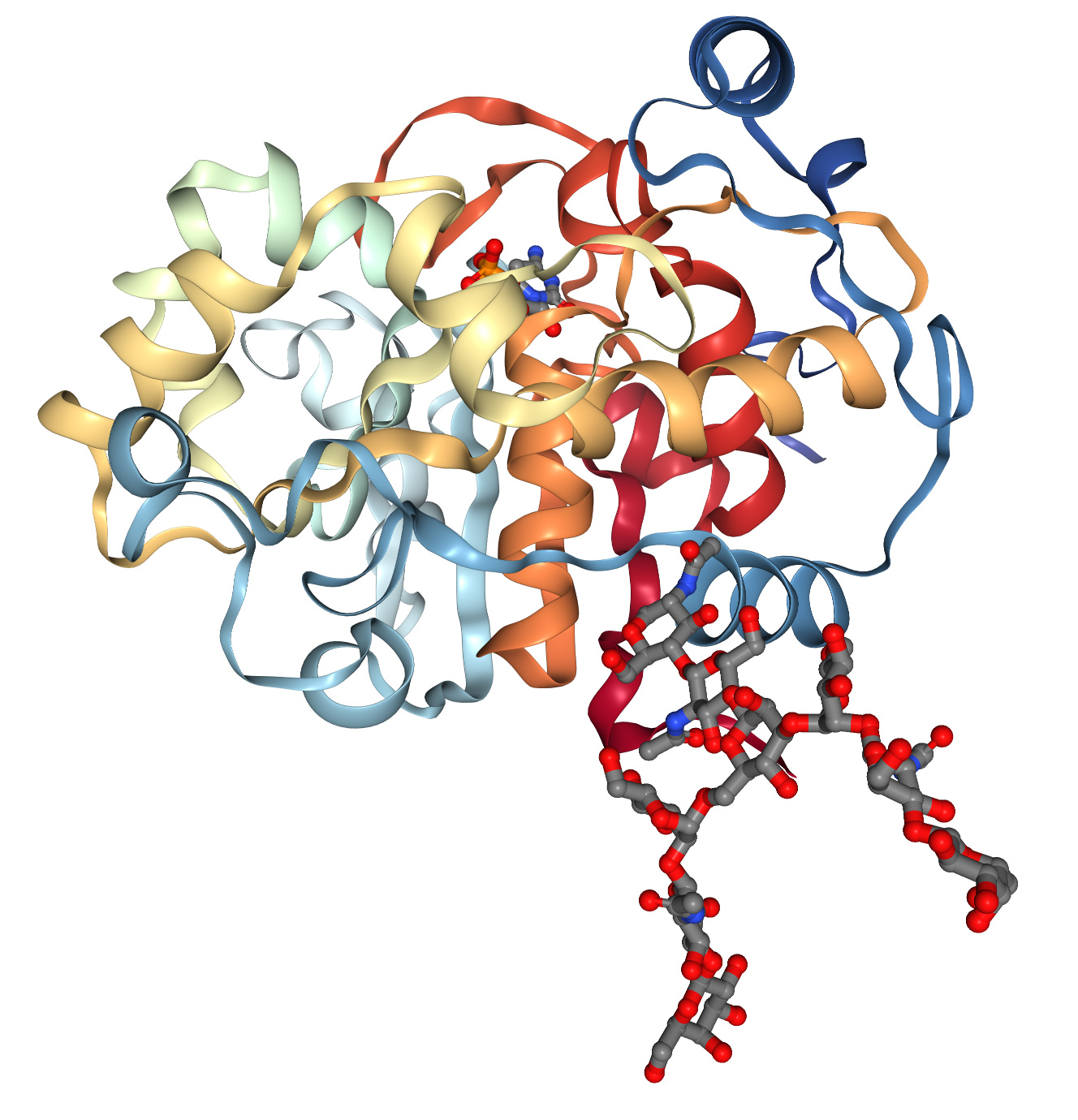
Այս տարվա Լասկերի հիմնական բժշկական հետազոտությունների մրցանակը շնորհվեց Դեմիս Հասսաբիսին և Ջոն Ջամփերին՝ ամինաթթուների առաջին կարգի հաջորդականության հիման վրա սպիտակուցների եռաչափ կառուցվածքը կանխատեսող AlphaFold արհեստական ինտելեկտի համակարգի ստեղծման գործում ունեցած ներդրման համար։
Նրանց արդյունքները լուծում են մի խնդիր, որը երկար ժամանակ անհանգստացնում էր գիտական հանրությանը և բացում են դուռ կենսաբժշկական ոլորտում հետազոտությունների արագացման համար: Սպիտակուցները կարևոր դեր են խաղում հիվանդությունների զարգացման գործում. Ալցհայմերի հիվանդության դեպքում դրանք ծալվում և կպչում են միմյանց. քաղցկեղի դեպքում դրանց կարգավորիչ գործառույթը կորչում է. բնածին նյութափոխանակության խանգարումների դեպքում դրանք դիսֆունկցիոնալ են. կիստիկ ֆիբրոզի դեպքում դրանք մտնում են բջջի սխալ տարածություն: Սրանք հիվանդություն առաջացնող բազմաթիվ մեխանիզմներից միայն մի քանիսն են: Սպիտակուցի մանրամասն կառուցվածքային մոդելները կարող են ապահովել ատոմային կոնֆիգուրացիաներ, խթանել բարձր կապակցվածության մոլեկուլների նախագծումը կամ ընտրությունը և արագացնել դեղերի հայտնաբերումը:
Սպիտակուցային կառուցվածքները սովորաբար որոշվում են ռենտգենյան բյուրեղագրության, միջուկային մագնիսական ռեզոնանսի և կրիոէլեկտրոնային մանրադիտակի միջոցով: Այս մեթոդները թանկ և ժամանակատար են: Սա հանգեցնում է սպիտակուցային կառուցվածքների եռաչափ տվյալների բազաների ստեղծմանը, որոնք պարունակում են ընդամենը մոտ 200,000 կառուցվածքային տվյալներ, մինչդեռ ԴՆԹ հաջորդականության որոշման տեխնոլոգիան ստեղծել է ավելի քան 8 միլիոն սպիտակուցային հաջորդականություններ: 1960-ականներին Անֆինսենը և իր գործընկերները հայտնաբերեցին, որ ամինաթթուների 1D հաջորդականությունը կարող է ինքնաբերաբար և կրկնվող կերպով ծալվել ֆունկցիոնալ եռաչափ կոնֆորմացիայի մեջ (Նկար 1Ա), և որ մոլեկուլային «շապերոնները» կարող են արագացնել և հեշտացնել այս գործընթացը: Այս դիտարկումները հանգեցնում են մոլեկուլային կենսաբանության 60-ամյա մարտահրավերի՝ սպիտակուցների 3D կառուցվածքի կանխատեսումը ամինաթթուների 1D հաջորդականությունից: Մարդու գենոմի նախագծի հաջողության շնորհիվ մեր կարողությունը՝ ստանալու 1D ամինաթթուների հաջորդականություններ, զգալիորեն բարելավվել է, և այս մարտահրավերը դարձել է ավելի հրատապ:
Սպիտակուցային կառուցվածքների կանխատեսումը դժվար է մի քանի պատճառներով: Նախ, յուրաքանչյուր ամինաթթվի յուրաքանչյուր ատոմի բոլոր հնարավոր եռաչափ դիրքերը պահանջում են մեծ ուսումնասիրություն: Երկրորդ, սպիտակուցները առավելագույնս օգտագործում են իրենց քիմիական կառուցվածքում լրացուցիչությունը՝ ատոմները արդյունավետ կերպով կարգավորելու համար: Քանի որ սպիտակուցները սովորաբար ունեն հարյուրավոր ջրածնային կապի «դոնորներ» (սովորաբար թթվածին), որոնք պետք է մոտ լինեն ջրածնային կապի «ակցեպտորին» (սովորաբար ազոտը կապված է ջրածնի հետ), շատ դժվար կարող է լինել գտնել կոնֆորմացիաներ, որտեղ գրեթե յուրաքանչյուր դոնոր մոտ է ակցեպտորին: Երրորդ, փորձարարական մեթոդների ուսուցման համար սահմանափակ օրինակներ կան, ուստի անհրաժեշտ է հասկանալ ամինաթթուների միջև հնարավոր եռաչափ փոխազդեցությունները՝ հիմնվելով 1D հաջորդականությունների վրա՝ օգտագործելով համապատասխան սպիտակուցների էվոլյուցիայի վերաբերյալ տեղեկատվությունը:
Ֆիզիկան առաջին անգամ օգտագործվել է ատոմների փոխազդեցությունը մոդելավորելու համար՝ լավագույն կոնֆորմացիայի որոնման մեջ, և մշակվել է մեթոդ՝ սպիտակուցների կառուցվածքը կանխատեսելու համար: Կարպլուսը, Լևիտը և Վարշելը 2013 թվականին արժանացել են քիմիայի Նոբելյան մրցանակի՝ սպիտակուցների հաշվողական մոդելավորման վերաբերյալ իրենց աշխատանքի համար: Այնուամենայնիվ, ֆիզիկայի վրա հիմնված մեթոդները հաշվողականորեն թանկ են և պահանջում են մոտավոր մշակում, ուստի ճշգրիտ եռաչափ կառուցվածքները հնարավոր չէ կանխատեսել: Մեկ այլ «գիտելիքների վրա հիմնված» մոտեցում է հայտնի կառուցվածքների և հաջորդականությունների տվյալների բազաների օգտագործումը՝ արհեստական բանականության և մեքենայական ուսուցման (AI-ML) միջոցով մոդելներ մարզելու համար: Հասաբիսը և Ջամփերը կիրառում են ինչպես ֆիզիկայի, այնպես էլ AI-ML տարրեր, բայց մոտեցման նորարարությունն ու կատարողականի թռիչքը հիմնականում բխում են AI-ML-ից: Երկու հետազոտողները ստեղծագործաբար համատեղել են խոշոր հանրային տվյալների բազաները արդյունաբերական մակարդակի հաշվողական ռեսուրսների հետ՝ AlphaFold-ը ստեղծելու համար:
Ինչպե՞ս գիտենք, որ նրանք «լուծել են» կառուցվածքային կանխատեսման հանելուկը։ 1994 թվականին հիմնադրվեց Կառուցվածքի կանխատեսման քննադատական գնահատման (CASP) մրցույթը, որը տեղի է ունենում երկու տարին մեկ՝ կառուցվածքային կանխատեսման առաջընթացը հետևելու համար։ Հետազոտողները կկիսվեն այն սպիտակուցի 1D հաջորդականությամբ, որի կառուցվածքը նրանք վերջերս են լուծել, բայց որի արդյունքները դեռևս հրապարակված չեն։ Կանխատեսողը կանխատեսում է եռաչափ կառուցվածքը՝ օգտագործելով այս 1D հաջորդականությունը, և գնահատողը անկախ կերպով գնահատում է կանխատեսված արդյունքների որակը՝ համեմատելով դրանք փորձարարի կողմից տրամադրված եռաչափ կառուցվածքի հետ (տրամադրված միայն գնահատողին)։ CASP-ն անցկացնում է իրական կույր վերանայումներ և գրանցում է մեթոդաբանական նորարարության հետ կապված պարբերական կատարողականի թռիչքները։ 2020 թվականին CASP 14-րդ համաժողովում AlphaFold-ի կանխատեսման արդյունքները ցույց տվեցին այնպիսի թռիչք կատարողականի մեջ, որ կազմակերպիչները հայտարարեցին, որ 3D կառուցվածքի կանխատեսման խնդիրը լուծվել է. կանխատեսումների մեծ մասի ճշգրտությունը մոտ էր փորձարարական չափումների ճշգրտությանը։
Ավելի լայն նշանակությունն այն է, որ Հասսաբիսի և Ջամփերի աշխատանքը համոզիչ կերպով ցույց է տալիս, թե ինչպես կարող է արհեստական բանականությունը, մեքենայական ուսուցումը (AI-ML) վերափոխել գիտությունը։ Դրա հետազոտությունները ցույց են տալիս, որ AI-ML-ը կարող է բարդ գիտական վարկածներ կառուցել բազմաթիվ տվյալների աղբյուրներից, որ ուշադրության մեխանիզմները (նման են ChatGPT-ում առկաներին) կարող են հայտնաբերել տվյալների աղբյուրներում հիմնական կախվածություններն ու փոխկապակցվածությունները, և որ AI-ML-ը կարող է ինքնուրույն դատել իր արդյունքի որակը։ AI-ML-ը, ըստ էության, գիտություն է։
Հրապարակման ժամանակը. Սեպտեմբերի 23-2023